| Indice Tema |
Si definiscono composti organici, tutti i composti del carbonio ad esclusione del monossido e del biossido di carbonio (anidride carbonica) e dei carbonati. Attualmente si conoscono più di 2 milioni di composti organici, e poiché se ne producono anche di artificiali, il loro numero è in continuo aumento. La capacità del carbonio di formare una così grande varietà di composti dipende sostanzialmente da tre fattori:
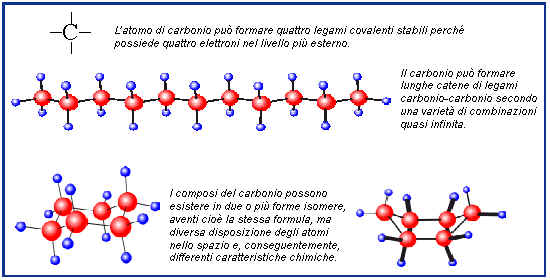
a) l’atomo di carbonio può formare quattro legami covalenti stabili perché possiede quattro elettroni nel livello più esterno;
b) il carbonio può formare lunghe catene di legami carbonio-carbonio secondo una varietà di combinazioni quasi infinita;
c) i composi del carbonio possono esistere in due o più forme isomere, aventi cioè la stessa formula, ma diversa disposizione degli atomi nello spazio e, conseguentemente, differenti caratteristiche chimiche.
In base alla natura degli atomi costituenti, i composti del
carbonio possono essere suddivisi in due grandi gruppi: quelli che contengono
soltanto carbonio e idrogeno (idrocarburi) e quelli che contengono anche
altri tipi di atomi, in particolare ossigeno e azoto.
Inoltre in base al tipo
di legame tra gli atomi di carbonio si distinguono composti saturi e
composti insaturi. Sono detti saturi i composti che presentano soltanto
legami semplici, mentre sono detti insaturi quelli che contengono anche legami
doppi o tripli tra atomi di carbonio. I composti insaturi sono instabili e
possono dar luogo a reazioni di addizione con vari reagenti che si uniscono ad
essi trasformando i doppi o tripli legami in legami semplici.
In base alla forma della molecola si possono distinguere i composti formati da una catena aperta più o meno ramificata di atomi di carbonio e quelli formati da una catena chiusa ad anello. I primi sono chiamati aciclici, i secondi ciclici.
Una struttura ad anello particolare, detta di tipo benzenico, contraddistingue il gruppo dei composti aromatici.

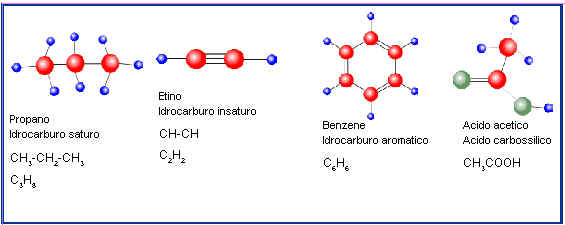
Rientrano tra i composti organici anche sostanze di importanza biologica che si possono raggruppare in quattro classi fondamentali: i glucidi, i lipidi, le proteine e gli acidi nucleici. Si tratta per lo più di molecole complesse dette macromolecole perché hanno dimensioni notevoli essendo costituite da migliaia di atomi. Molte macromolecole biologiche sono polimeri formati dall’unione di composti organici più piccoli detti monomeri. I monomeri si uniscono a formare i polimeri mediante una reazione di condensazione che comporta la perdita di una molecola d’acqua per ciascun legame che si forma. La sintesi di un polimero richiede energia ed è regolata da diversi enzimi.
I polimeri possono essere degradati nei monomeri che li compongono mediante una reazione di idrolisi consistente nella rottura dei legami tra i monomeri ad opera di specifici enzimi con aggiunta di una molecola di acqua per ogni legame che viene scisso.
I carboidrati o glucidi sono composti organici formati da carbonio, idrogeno e ossigeno; essi rappresentano le principali molecole di riserva energetica dei viventi ma entrano anche nella costituzione di molti componenti strutturali delle cellule. I glucidi sono polimeri di molecole semplici (monomeri) dette zuccheri.
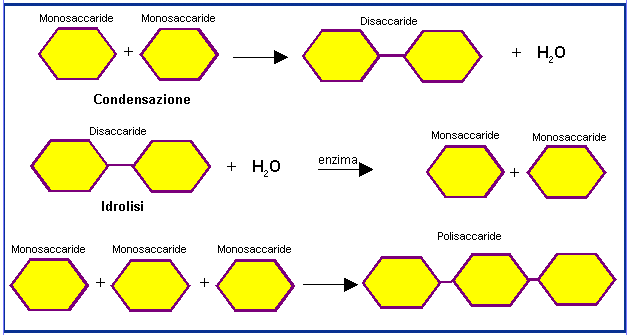
A seconda del numero di molecole di zucchero che contengono si distinguono monosaccaridi o zuccheri semplici, disaccaridi formati da due molecole di zucchero unite da un legame covalente e polisaccaridi formati da molte molecole di zucchero legate tra loro.
I carboidrati possono combinarsi con le proteine per formare le glicoproteine e con i lipidi per formare i glicolipidi: glicolipidi e glicoproteine sono presenti nella membrana delle cellule.
I monosaccaridi possono esere rappresentati con la formula generica (CH
2O)n, dove n è un numero intero; nella molecola sono presenti uno o più gruppi ossidrili (OH) e un gruppo aldeidico (CHO) oppure un gruppo chetonico (CO). In soluzione acquosa le molecole dei monosaccaridi assumono la forma chiusa ad anello.I disaccaridi derivano dalla condensazione di due molecole di
monosaccaridi uguali o diversi. Tra le due molecole si forma un ponte con una
molecola di ossigeno; si forma cioè un legame glicosidico.
Il
saccarosio si estrae dalla barbabietola e dalla canna da zucchero ed è
largamente usato come dolcificante nell’alimentazione; la sua molecola risulta
dall’unione di una molecola di glucosio e una di fruttosio.
Il
maltosio (glucosio + glucosio) è contenuto nell’orzo mentre il
lattosio (galattosio + glucosio) è contenuto nel latte.
I polisaccaridi si ottengono dalla condensazione di numerose
molecole dello stesso zucchero. Polisaccaridi diversi possono essere costituiti
dallo stesso monosaccaride; differiscono in tal caso per il tipo di legame
glicosidico (detto alfa o beta) e per l’eventuale presenza di catene
ramificate.
L’amido costituisce la principale riserva energetica delle
piante; è un polimero formato da molte molecole di

I lipidi sono composti formati da carbonio, idrogeno, ossigeno e, in qualche caso fosforo e azoto. Sono sostanze grasse che svolgono molti compiti nella cellula:
- fungono da riserve di energia;
- costituiscono un importante componente della membrana cellulare;
- accumulati in determinate parti del corpo proteggono dagli urti e assicurano l’isolamento termico;
- regolano importanti funzioni vitali.
I lipidi non si sciolgono nell’acqua ma sono solubili in alcool, etere, e altri solventi organici.
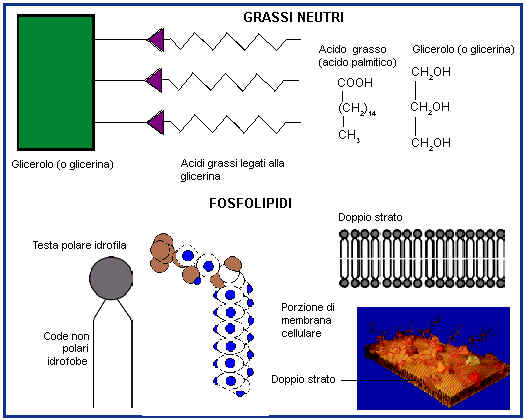
I grassi neutri sono i lipidi più abbondanti negli
esseri viventi; essi possono fornire più del doppio dell’energia fornita dai
carboidrati. I grassi neutri sono costituiti da glicerolo e una o più molecole
di acidi grassi.
Il glicerolo è un alcool formato da tre atomi di
carbonio e da tre gruppi ossidrilici (OH). Gli acidi grassi sono catene
contenenti un numero di atomi di carbonio compreso tra 14 e 22. Se tra gli atomi
di carbonio esistono soltanto legami semplici l’acido grasso viene detto
saturo perché gli atomi di carbonio non possono formare altri legami; se
invece compaiono uno o più doppi legami l’acido grasso viene detto
insaturo perché gli atomi di carbonio con il doppio legame possono
formare altri legami. Gli acidi grassi con un solo doppio legame vengono detti
monoinsaturi, mentre quelli con più di un doppio legame sono detti
poliinsaturi.
Quando una molcola di glicerolo si combina con una molecola di acido grasso si forma un monogliceride, se gli acidi grassi sono due si forma un digliceride mentre se gli acidi grassi sono tre si forma un trigliceride.
Il legame che si instaura tra una molecola di glicerolo e una di un acido grasso è covalente e prende il nome di legame estere. Nell’organismo, durante la digestione i grassi neutri vengono trasformati nelle molecole che li compongono attraverso una reazione di idrolisi che porta alla rottura del legame estere.
I fosfolipidi fanno parte della struttura della membrana delle cellule. Un fosfolipide è formato da una molecola di glicerolo unita a due acidi grassi e legata a un gruppo fosfato (PO
4-) a sua volta legato ad una base organica (colina) generalmente contenente azoto. La molecola risulta formata da una "testa" polare e idrofila e da due code non polari e idrofobe . La "testa" è proprio il gruppo fosfatico carico negativamente e le due "code" sono formate dal glicerolo e dalla base organica. I lipidi con questa caratteristica vengono in generale detti anfipatici.In acqua le molecole dei fosfolipidi tendono ad aggregarsi formando un doppio strato con le teste polari rivolte verso l’acqua e le code idrofobe non polari rivolte in direzione opposta.
Il doppio strato può formare lamine che tendono a rinchiudersi su se stesse delimitando un ambiente interno acquoso separato dall’esterno. Una struttura del genere viene denominata micella.
Gli steroidi sono composti formati da quattro anelli carboniosi legati tra loro che possono essere completati da una coda di idrocarburi e possono contenere anche uno o più gruppi OH. Il rappresentante principale di questo gruppo di lipidi è il colesterolo. Questo composto è uno dei costituenti principali della membrana cellulare e, insieme ai fosfolipidi e ai glicolipidi ne influenza la stabilità, la mobilità e la permeabilità. Viene inoltre immagazzinato nelle ghiandole surrenali, nei testicoli e nelle ovaie per essere trasformato nei vari ormoni steroidei (ormoni sessuali o corticosteroidi).
Gli amminoacidi sono composti organici caratterizzati dalla presenza, nella loro molecola, di un gruppo funzionale acido, il carbossile COOH, di un gruppo funzionale basico rappresentato dal gruppo amminico NH
2 e di un radicale. In natura esistono soltanto una ventina di amminoacidi.Gli aminoacidi si combinano tra di loro mediante un legame covalente, detto legame peptidico, tra il gruppo carbossilico di una molecola e il gruppo amminico di un’altra. Quando si combinano due aminoacidi si forma un dipeptide; una catena più lunga viene chiamata polipeptide. Una proteina è formata da uno o più polipeptidi. Le proteine sono il principale costituente delle cellule, formando più del 50% del peso secco degli animali.

Secondo i tipi, la quantità e l’ordine di allineamento degli amminoacidi si formano proteine con differenti caratteristiche e funzioni. Utilizzando soltanto 20 differenti aminoacidi, una cellula può costruire migliaia di differenti proteine, ognuna delle quali ha un proprio ruolo nella cellula.
Si chiamano essenziali gli amminoacidi che un organismo animale non è in grado di sintetizzare e deve necessariamente assumere con la dieta. Nell’uomo gli amminoacidi essenziali sono una decina.
Il peso molecolare delle proteine può variare da poche centinaia a più di un milione. Le proteine sono specifiche per ciascuna specie e per ciascun organo della stessa specie. Nel corpo umano ci sono 30.000 differenti proteine. Le funzione principale di queste molecole è quella di costruire e mantenere le cellule, ma la loro demolizione chimica produce anche energia.
Le quasi infinite combinazioni nelle quali gli aminoacidi possono unirsi, e le varie forme che assumono, spiegano la grande varietà di funzioni che le proteine possono svolgere nella materia vivente:
- concorrono a formare l’impalcatura del corpo;
- svolgono una funzione catalitica (enzimi);
- fungono da mezzo di trasporto di altre molecole;
- sono responsabili del movimento;
- hanno compiti protettivi;
- svolgono funzioni di regolazione;
- fungono da riserva di sostanze nutritive;
- controllano il pH del sangue.
Le catene polipeptidiche che formano una proteina sono
attorcigliate o ripiegate per formare una macromolecola.
Quando le catene
polipeptidiche formano lunghe fibre si hanno le proteine fibrose; quando le
catene polipetidiche sono ripiegate in una forma compatta quasi sferica si hanno
le proteine globulari.
Nella molecola proteica si possono distinguere quattro livelli di organizzazione denominati strutture.
La struttura primaria di una proteina è la sua sequenza di amminoacidi.Cambiamenti della struttura tridimensionale di una proteina possono alterare la sua attività biologica. Quando una proteina viene scaldata o trattata con prodotti chimici la sua struttura terziaria diventa disordinata e le catene peptidiche si aprono per dare una conformazione meno ordinata. Questo srotolamento è associato alla perdita dell’attività bilogica della proteina. Tale cambiamento di configurazione e la conseguente perdita di attività biologica vengono definiti denaturazione della proteina.
Gli enzimi
Perché qualunque reazione possa avvenire devono essere prima di tutto destabilizzati i legami chimici tra gli atomi dei reagenti. Per esempio, se la reazione comporta la rottura di un legame covalente, gli atomi che formano il legame devono prima scostarsi per essere meno stabili. Prima che un legame sia forzato abbastanza per rompersi deve essere fornita una certa quantità di energia, definita energia di attivazione. I sistemi viventi per destabilizzare i legami chimici nelle reazioni metaboliche impiegano i catalizzatori.
I catalizzatori sono sostanze chimiche che accelerano le velocità delle reazioni senza influenzare i prodotti della reazione e senza essere alterati o distrutti come conseguenza della reazione. I catalizzatori del mondo vivente si chiamano enzimi.
Gli enzimi sono sostanze di natura proteica specializzate ciascuna nella catalisi di una specifica reazione chimica del metabolismo degli organismi viventi. Attualmente sono stati identificati più di 700 enzimi.
Gli enzimi vengono suddivisi in ampie categorie, in base al tipo di reazione che controllano. Ad esempio, gli enzimi idrolitici catalizzano le reazioni in cui una sostanza viene degradata in composti più semplici, in presenza di acqua; gli enzimi ossidanti, o ossidasi, catalizzano le reazioni di ossidazione; e quelli riduttori, o riduttasi, catalizzano le reazioni di riduzione, in cui viene eliminato ossigeno.
Alcuni enzimi, come la pepsina e la tripsina che determinano la digestione delle proteine, sono in grado di catalizzare molte reazioni diverse, mentre altri, come le ureasi, sono specifici per una singola reazione. Alcuni enzimi regolano reazioni in cui viene liberata l’energia necessaria, ad esempio, al battito del cuore e all’espansione e alla contrazione dei polmoni; altri facilitano la conversione dello zucchero e degli alimenti nelle varie sostanze utilizzate dall’organismo per fabbricare i tessuti.
Per essere attivi molti enzimi richiedono la presenza di piccoli gruppi non proteici chiamati cofattori. In alcuni casi questi cofattori sono ioni metallici (ferro, rame, zinco, magnesio, potassio, calcio), in altri casi si tratta di sostanze organiche dette coenzimi. Tutti i coenzimi contengono gruppi derivati da vitamine, composti che devono essere forniti con la dieta.
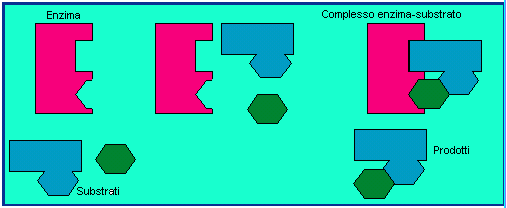
In generale, l’attività catalitica è svolta solo da una piccola porzione della molecola dell’enzima, detta sito attivo, capace di legare a se il substrato, cioè le molecole che devono reagire. Il substrato si lega all’enzima attraverso legami deboli e l’unione dell’enzima col substrato forma un complesso enzima-substrato (complesso ES). Il complesso ES si dissocia rapidamente, ma durante questo brevissimo tempo, l’enzima fornisce un ambiente chimico idoneo a forzare i legami.
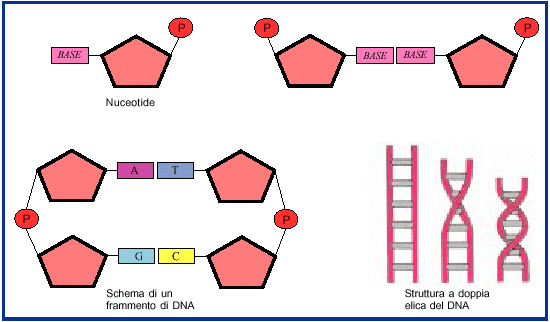
Gli acidi nucleici sono dei polimeri i cui monomeri sono detti nucleotidi. Un nucleotide è costituito da tre elementi: una base azotata, uno zucchero con cinque atomi di carbonio (ribosio o desossiribosio) e un gruppo fosfato. Una sequenza di nucleotidi uniti tra loro da ponti fosfato tra il ribosio di un nucleotide e quello del nucleotide adiacente prende il nome di polinucleotide.
DNA (dall'inglese DeoxyriboNucleic Acid, o acido desossiribonucleico) è la sigla dell'acido desossiribonucleico, presente in tutte le cellule come portatore dell'informazione genetica. Dai batteri fino agli animali e alle piante, tutti gli esseri viventi hanno come codice genetico il DNA che si trova all'interno di ogni singola cellula e controlla tutte le loro attività vitali.
Il modello dell'acido desossiribonucleico è stato sviluppato nel 1953 da James Watson and Francis Crick.
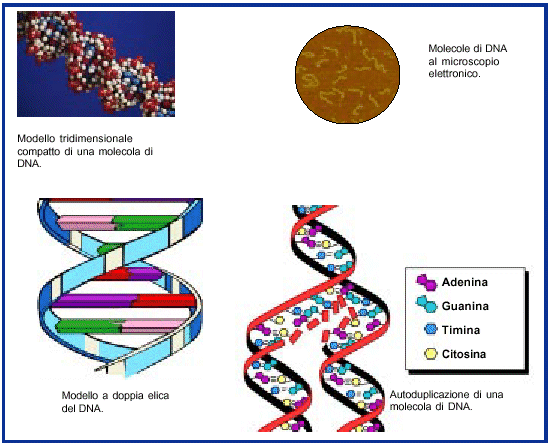
La molecola del DNA è organizzata in due catene di polinucleotidi avvolti a spirale l'una intorno all'altra in modo da formare una doppia elica. Nel DNA ogni nucleotide è formato da una molecola di desossiribosio (D), da una base azotata che può essere adenina A, guanina G, citosina C o timina T e da un gruppo fosfato. Le due catene si legano attraverso le basi azotate con un legame relativamente debole detto "legame idrogeno". L'appaiamento avviene solo tra le adenine di una catena e le timine dell'altra (A-T) e tra le guanine di una catena e le citosine dell'altra (G-C). Poiché non è possibile l'unione con una combinazione differente, l'allineamento delle basi di una metà della catena, automaticamente stabilisce anche la sequenza delle basi dell'altra. Possiamo paragonare questa struttura a quella di una scala a chiocciola: i montanti della scala sono rappresentati dall'alternanza del desossiribosio, e del gruppo fosfato. I pioli che uniscono i due montanti sono rappresentati dalle molecole delle basi azotate.
Il DNA porta "scritte" in forma codificata tutte le informazioni necessarie per il corretto svolgimento delle attività biologiche delle cellule e degli organismi da esse composti. Il codice utilizzato, noto come codice genetico, è rappresentato dall'ordine in cui si susseguono le basi lungo la catena. Tre basi del DNA costituiscono l'unità del codice genetico; ogni unità contiene le istruzioni per formare un aminoacido. Basandosi sulle informazioni del DNA e con l'aiuto di particolari enzimi le cellule possono costruire le proteine.
Il DNA si autoduplica
Il DNA è la molecola che rende possibile la vita grazie ad una sua caratteristica fondamentale: la capacità di autoriprodursi. Duplicando se stesso il DNA può trasmettere il suo codice genetico a tutte le cellule dell'organismo di cui fa parte e ai suoi discendenti. Il processo di duplicazione del DNA è chiamato replicazione. É proprio la struttura a doppia elica che permette la replicazione del DNA con relativa semplicità: le due eliche si separano gradualmente e ciascuna diventa uno stampo sul quale, con l'aiuto di particolari enzimi si riforma l'elica complementare. Alla fine del processo si ha la formazione di due doppie eliche uguali.
La replicazione del DNA è detta semiconservativa perché ognuna delle due molecole figlie è costituita da un filamento del DNA originario (conservato) e da un filamento sintetizzato ex-novo.
L'intero processo richiede energia e molti enzimi tra i quali un gruppo di enzimi noti come DNA polimerasi che catalizza la sintesi vera e propria. La replicazione del DNA è estremamente precisa: la DNA polimerasi è in grado di accorgersi se ha aggiunto un nucleotide sbagliato al filamento in costruzione e di rimediare all'eventuale errore.
Presente nel nucleo e nel citoplasma di tutti gli organismi, l'acido ribonucleico è un polinucleotide a singola elica costituito da una sequenza di nucleotidi in ciascuno dei quali sono presenti un gruppo fosfato, un ribosio e una base azotata che può essere adenina A, guanina G, citosina C o uracile U. I nucleotidi sono uniti tra di loro da ponti di fosfato tra il ribosio di un nucleotide e quello del nucleotide adiacente. Esistono diversi tipi di RNA, ognuno dei quali è preposto ad una funzione specifica (RNA messaggero o m-RNA, RNA di trasferimento o t-RNA, RNA ribosomiale o r-RNA). La presenza dell'uracile al posto della timina e del ribosio al posto del deossiribosio distingue chimicamente l’RNA dal DNA. In alcuni virus (retrovirus) l’RNA costituisce l’unica molecola contenente informazione genetica.
L’ATP (adenisin trifosfato) è il più importante di un gruppo di composti, comunemente chiamati "composti ad alta energia", che possiedono la proprietà di rilasciare molta energia quando donano una parte di se stessi all’acqua o ad altri accettori. Le parti donate possono essere atomi, gruppi di atomi o soltanto coppie di elettroni. L’ATP è la fonte principale di energia per processi di vario tipo come la bioluminescenza, la contrazione muscolare, il trasporto di ioni attraverso la membrana cellulare, la sintesi di carboidrati, grassi, proteine ed amminoacidi e la fissazione di azoto ed anidride carbonica.
L'ATP è la fonte principale di energia per svariati processi come la bioluminescenza, la contrazione muscolare, il trasporto di ioni attraverso la membrana cellulare, la sintesi di carboidrati, grassi, proteine ed amminoacidi e la fissazione di azoto ed anidride carbonica.
In particolare, l’ATP consente di trasferire energia chimica da una reazione che libera energia ad una reazione che richiede energia, tramite la cessione e l’acquisto di gruppi fosforici. L’ATP funziona da trasportatore di energia in tutti gli organismi viventi dai batteri ai funghi alle piante agli animali incluso l’uomo. L’ATP cattura l’energia chimica rilasciata dalla combustione dei nutrienti (reazioni esoergoniche) e la trasferisce in reazioni che richiedono energia (endoergoniche) e che sono necessarie alla cellula per svolgere le sue funzioni e per la sintesi di molecole biologiche. Quando l’ATP viene trasformato in ADP (adenosin difosfato) e fosfato inorganico (Pi), viene liberata energia che può essere utilizzata, in presenza di specifici enzimi, per dirigere i vari processi cellulari che richiedono energia.
La nicotinamide adenindinucleotide (NAD) svolge un ruolo fondamentale nelle reazioni accoppiate di ossido-riduzione che avvengono all’interno delle cellule.Può esistere in forma ossidata NAD
+ che si trasforma nella forma ridotta NADH. Gli elettroni dell’atomo di idrogeno della forma ridotta possono essere trasferiti ad altre molecole insieme all’energia ad essi associata.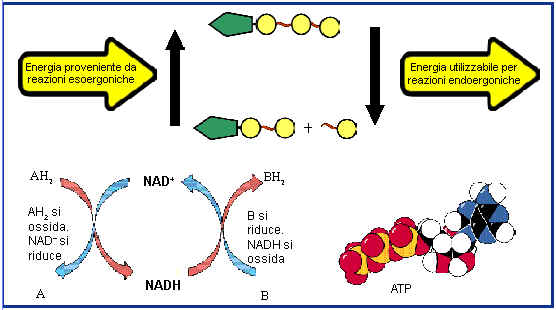
G. Picciolo novembre 2000
Tutti i diritti riservati. Nessuna parte dei documenti
contenuti in questo sito può essere pubblicata o comunque distribuita in
qualsiasi forma. È consentito l'uso didattico. © Giuseppe Picciolo ottobre 2000
-
ClipArt e foto tratte dalle raccolte Corel Gallery e Microsoft
Office